原子番号 電子の数 192423-原子番号 と 電子の数
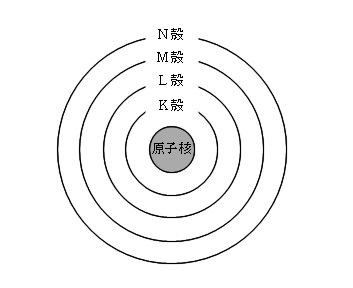
S電子からf電子の軌道の数は、それぞれ 1,3,5,7となります。 族番号 1~18は新IUPACによる族番号で、1A~7A(ⅠA~ⅦA)・8(Ⅷ)・1B~7B(ⅠB~ⅦB)・0は従来の族名です。 原子殻 K殻は1s、L殻は2s~2p、M殻は3s~3d、N殻は4s~4fとなります。原子は原子番号と同じ数の電子を持っています。 その電子は電子殻に存在し、そ れぞれの電子殻に入る最大電子数は、K殻に2個、L 殻に8個、M殻原子の大きさとは,原子核の 周りを回る電子の分布範囲である。これがなぜ 元素の種類にあまり依存しないのかは,以下の ように考えることができる。 原子番号Z の中性の原子では,原子核が有 する電荷は+Ze(e は素電荷)であり,核外電 子数もZ 個で

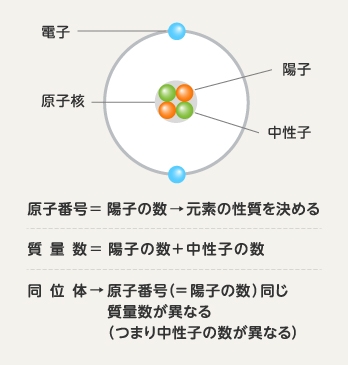
原子核や質量数 同位体の語呂合わせ 陽子数 中性子数 原子番号など 18h30大学入学共通テスト試行調査第2回第1問c 問5 語呂合わせで高校化学 大学入試ゴロ化学
原子番号 と 電子の数
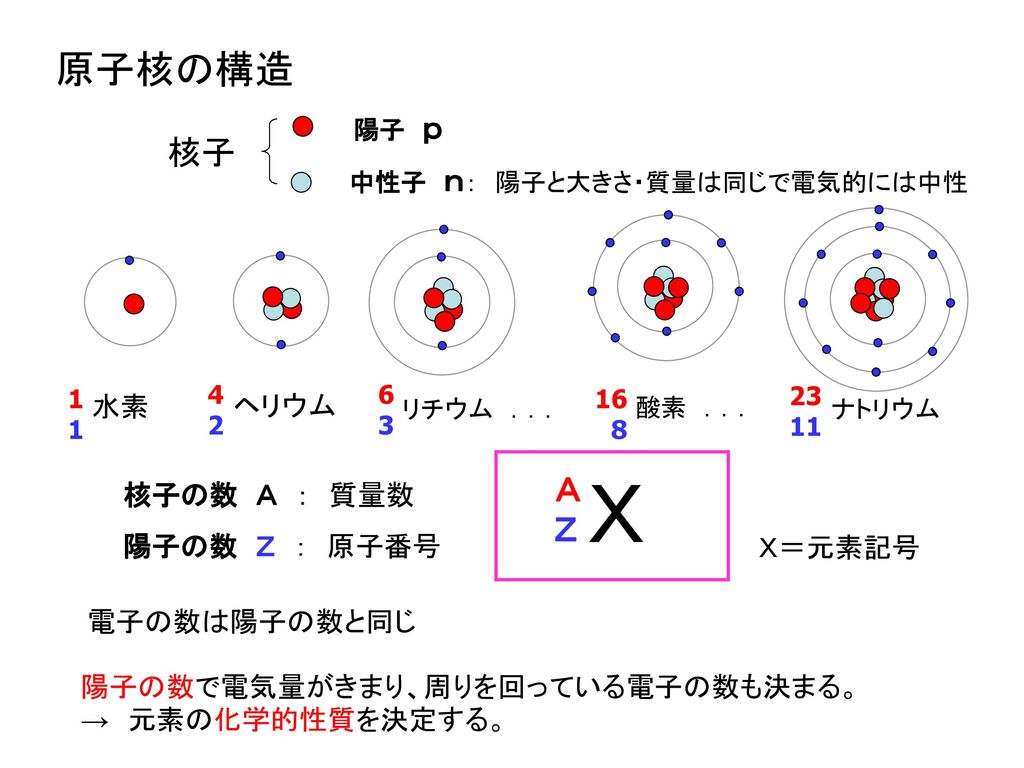
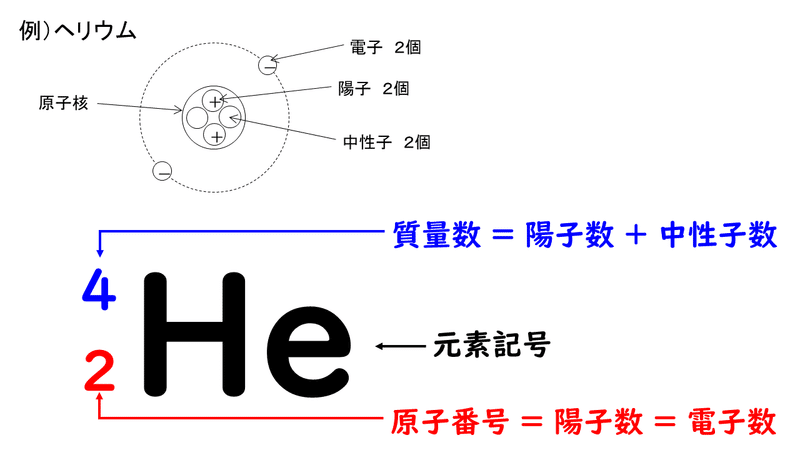
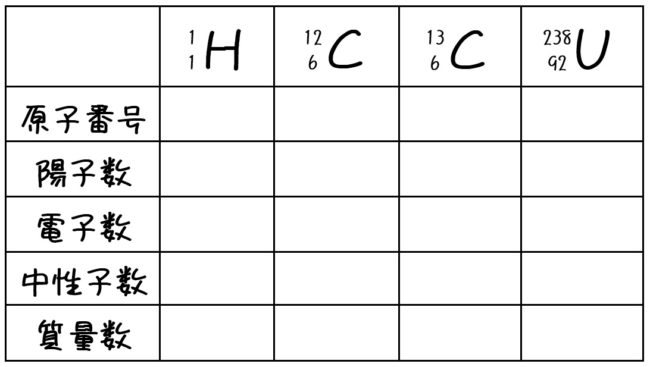
原子番号 と 電子の数-・原子においては,「原子番号 = 陽子の数 = 電子の数」が成り立つ。 ・「質量数 = 陽子の数 中性子の数」の関係がある。 ・元素記号の左上に質量数,左下に原子番号を書く。原子番号原子番号Zの原子の電子配置が決まっているとき、 原子番号 Z1の原子については、新たにつけ加わる 1個の電子に、空いている軌道のうち エネルギエネルギ の ー の 最も低い軌道の量子数 を割り当てる。 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s
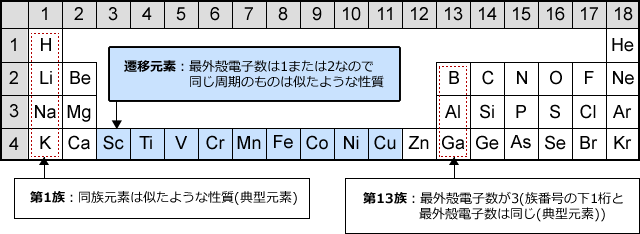



化学講座 第3回 元素の周期表 私立 国公立大学医学部に入ろう ドットコム
原子量(u) 英語名の由来 電子 配置図 1 H 水素 Hydrogen Hydrogenium 1 1 (7) 性質:希 hydro(水)gennao(生じる) 100 2 He ヘリウム Helium Helium 1 18 (2) 場所:太陽上に発見、希 helios(太陽) 467 3 Li リチウム Lithium Lithium 2 1 6941(2)物質の化学的性質は原子番号、すなわち核の周りにある電子数によって決定づけられ、それぞれ元素名が付けられています。 それを表にしたものが元素の 周期表 です。 同じ原子番号であっても核内の中性子数が異なる物をアイソトープ (isotope)といいます。 自然界に安定して存在するものと加速器や原子炉で作られる安定でない放射性アイソトープ (radio isotope)とが甥 原子核のまわりの電子の数が原子番号と異なる粒子も存在し,そのような粒子をイオンとよ ぶ。〇 原子は電気的に中性であり,電子の数と陽子の数(=原子番号)が等しい。電子の 数が増減することによって,原子は陰イオンや陽イオンになる 。
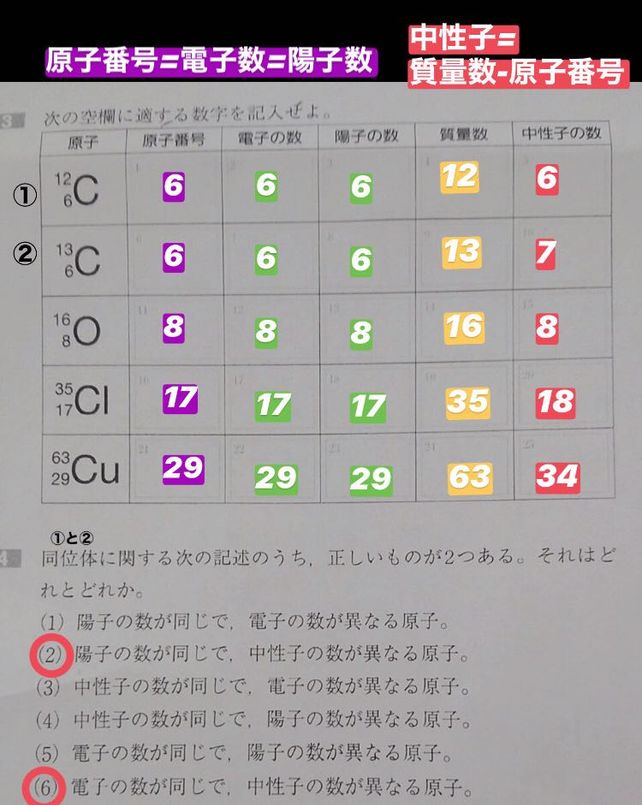
その左側に、「4」、「2」という数字が書かれていますね。 まず、下にある 「2」 に注目します。 この数字のことを 「原子番号」 といいます。 野球選手にとっての「背番号」が、原子の「原子番号」なのです。 背中にある番号が「背番号」、 原子の番号なのだから「原子番号」 なのですね。 とても覚えやすいですね。 この原子番号は、原子ごとに別々のもの問1 次の原子の陽子の数,中性子の数,電子の数をそれぞれ求めよ。 (1)11Na 23 (2) Cl 17 35 原子番号=陽子の数=電子の数 中性子の数=質量数-原子番号 で求める。 (1) 陽子の数 11,中性子の数 12,電子の数 11 (2) 陽子の数 17,中性子の数 18,電子の数 17 ( 質量原子の化学的性質は電子の個数、すなわち原子番号によって決定されます。原子 番号の同じ原子の集団を元素といいます。 2原子量と分子量 簡単にいうと、同位体の質量数の平均(加重平均)を原子量といいます。原子量
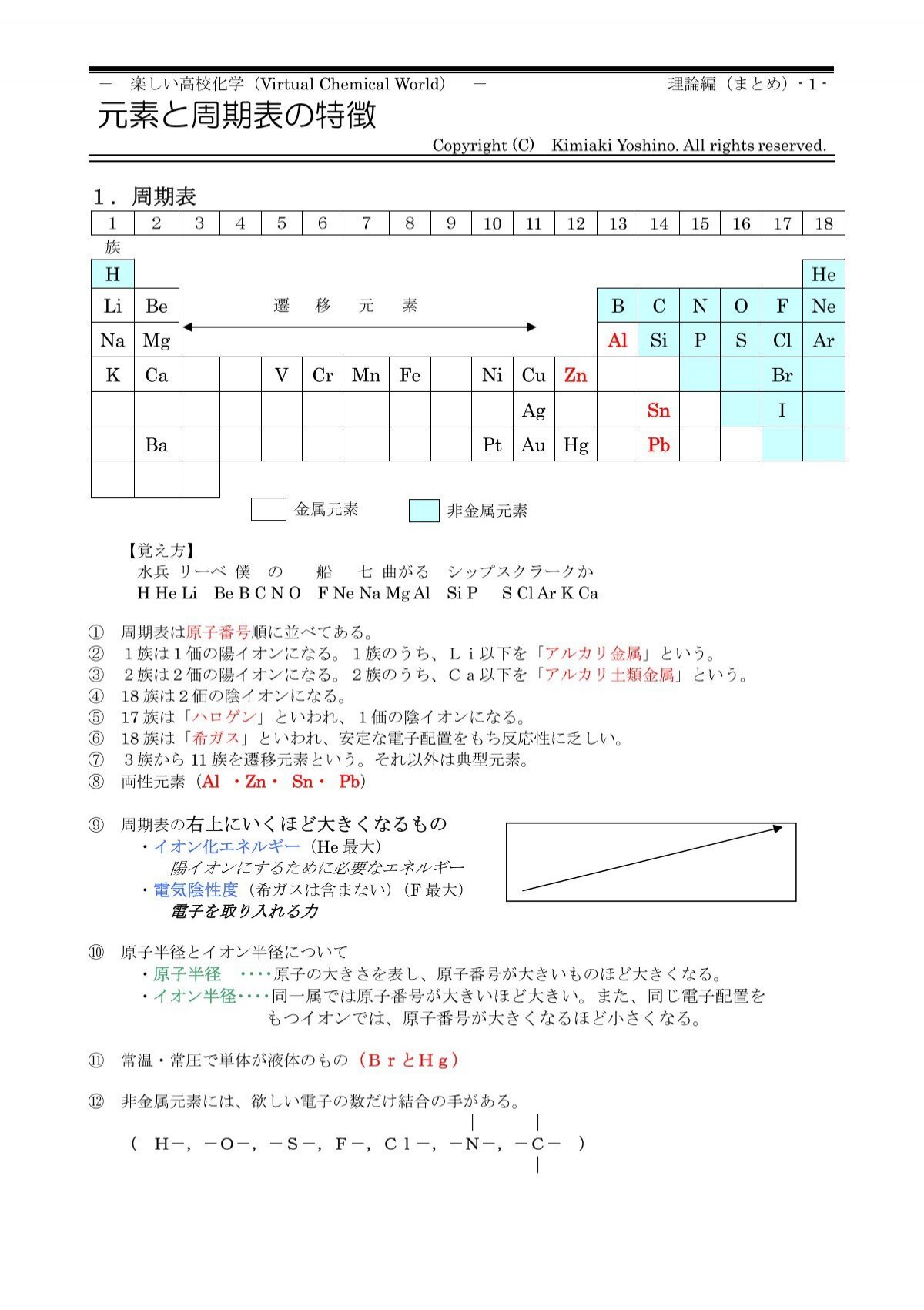
原子番号 (げんしばんごう、 英語 atomic number )とは、 核種 を区別する量の一つで、 原子核 の中にある 陽子 の個数である。 電荷 を帯びていない中性 原子 においては、原子中の 電子 の数に等しい。 通常は記号 Z で表されるが、これは「数」や「番号従って、原子番号(陽子数)から正電荷数(イオン価数)を引いた値が、このイオンに残っている電子数になります。 例:Ca 2 はプラス2の電荷を帯びているため、原子から電子が2つ放出された陽イオンになります。Effective atomic number 化合物中で、一つの 原子 に注目したとき、その原子に所属する電子の数を、その原子の有効 原子番号 という。




中性子 電子 質量数の数はそれぞれどうやって求めるんですか 陽子の数 原子番号なのは Clear



Www Zkai Co Jp Wp Content Uploads Sites 15 19 09 Qcs5a1z1a2 1 Pdf
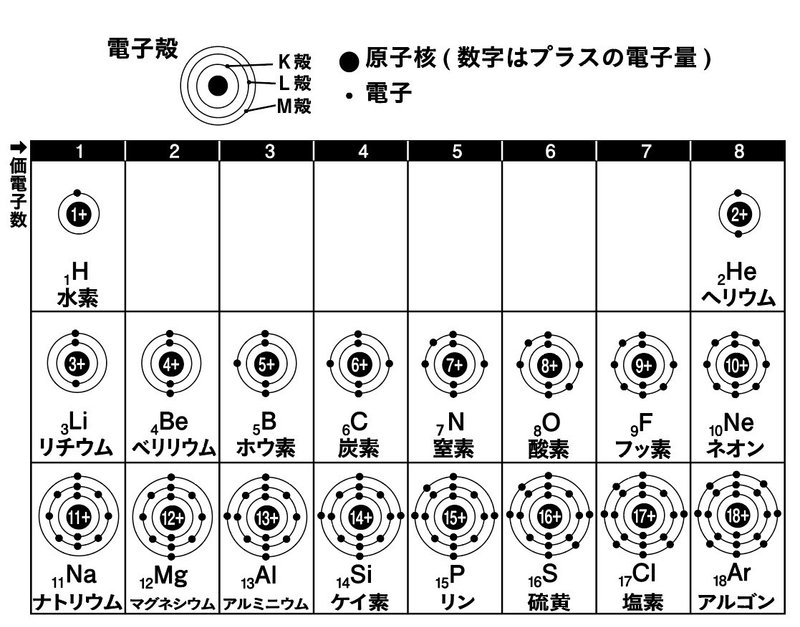
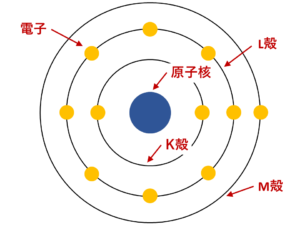
原子番号と質量数の表し方 ( 質量数 ) 例 4 ( 原子番号 ) 2 この場合,質量数は4 で 原子番号は2 である。 問 次の原子に含まれる陽子の数,電子の数,中性子の数をそれぞれ求めよ。 (1) 23Na 11 (2) 40Ar 18 中性子の数=質量数-原子番号で求める。「原子番号 = 電子の数」 でしたよね? (これも大事なコツですよ!) 電子の数は、 「2個」で安定し、(※ 内側の軌道に 2個 ) 「10個」で安定し、(※ 内側に 2個 、2番目に 8個 ) 「18個」で安定します。(※ 3番目の軌道に 8個 ) 周期表で確認すると、 LINE Pocket 図解高校化学基礎より、原子の構造、分子との関係性、原子と元素の違い、陽子・中性子・電子・質量数・原子番号の関係性と違い、原子核とは何かなど、具体的に図を示しながら丁寧に解説します。 僕は10年以上にわたりプロとして個別



1




質量数とは 求め方 みんなが知りたい2つの疑問を解消 高校生向け受験応援メディア 受験のミカタ
原子番号は、問題の要素を構成する陽子の数を示します。 たとえば、ホウ素(b)の原子番号は5です。したがって、5つのプロトンがあります。 電子の数を決定します。 原子核には、正に帯電した粒子である陽子が含まれます。電子は負に帯電した粒子です。原子の原子番号は、陽子(および電子)の数に基づいています。 安定した(中性の)原子は、常に同じ数の陽子と電子を持ちます。 原子量は陽子と中性子の両方の組み合わせです。 たとえば、炭素は6つの陽子(および電子)で構成されているため、原子つ電子数は原子核中の陽子数と等しい.したがって,原子核中の陽子数が中性の 原子中の電子数を決め,化学的性質すなわち元素としての属性を決める.そこで, 陽子数を原子番号とし,陽子数がじであるときの原子に一つの元素記号を与え る. 原子番号




電子の総数は陽子の数で計算するのでか Clear




イオン化エネルギー 電子親和力 電気陰性度のグラフの違いを区別せよ 化学受験テクニック塾
電気的に中性な原子は、原子核の中の 陽子と同じ数の軌道電子を持っています。 原子はそれぞれの原子番号の違いによってまったく個性(化学的性質) が違うため別々の名前が与えられています。例えば、原子番号1は水素、原子番号3,中性子数4,質量数7 7 Li のリチウム原子は右のように表記します。 3 原子番号=陽子数=電子数,質量数=陽子数+中性子数 でしたね。 Liはリチウムを表す元素記号ですね。 左下の3は原子番号(陽子数と電子数もこれと同じ),左上の7はページの上に戻る ©0121 NetAdvance Inc All rights reserved




原子核で元素を読み解く 小林良彦のブログ
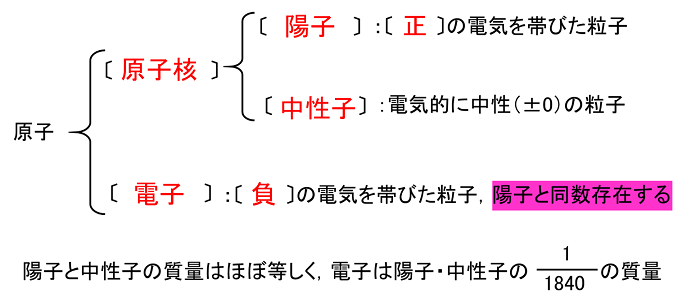



原子とその構造
化学 最外殻電子の数 初歩の化学を学習しております。最外殻電子の数は8個までしか入らないそうですが、原子番号21のスカンジウムはM殻に9個入るとテキストに書いてありました。このあたり、理解がイマイ 質問No




質量数とは 求め方 みんなが知りたい2つの疑問を解消 高校生向け受験応援メディア 受験のミカタ




同じ電子配置では原子番号が増えるほどイオン半径が小さくなるメカニズム




高校化学基礎 同じ電子配置のイオン 映像授業のtry It トライイット



実習5 原子の構造 3年理科 化学 Takaの授業記録18
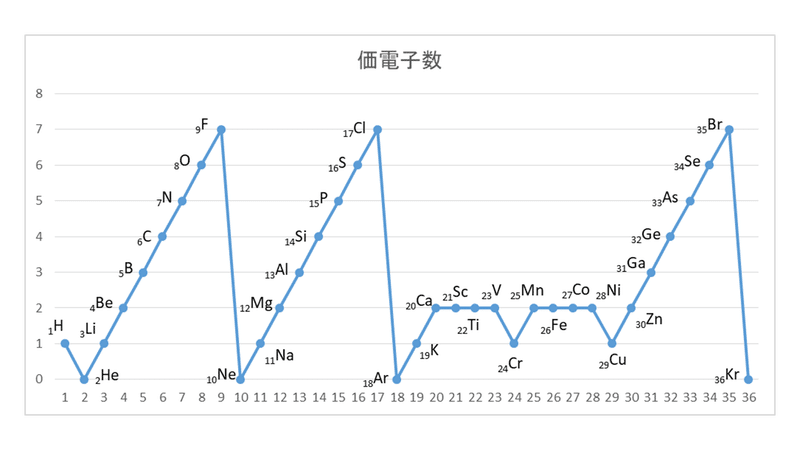



1 6 元素の周期律と周期表 おのれー Note




原子の構造 陽子 中性子 電子 原子核 質量数 原子番号の数と関係 化学のグルメ




原子の構造 原子番号と質量数の関係 Dr あゆみの物理教室



標準第1講



化学 原子の構造 技術情報館 Sekigin 原子の構造 原子番号 周期表 電子構造 電子軌道 主量子数 方位量子数 磁気量子数 最外殻電子 フェルミ粒子 パウリの排他原理などを紹介



原子番号1 の電子配置 価電子の数を覚えなければならないので Yahoo 知恵袋



なんとなくわかる高校化学 元素と周期表



原子番号 電子の数であるのに 同じ電子配列ってどういう事ですか 原子番 Yahoo 知恵袋




原子の構造と原子番号と電子数および質量数




株式会社 マテリアルハウス 金属あれこれ 周期表
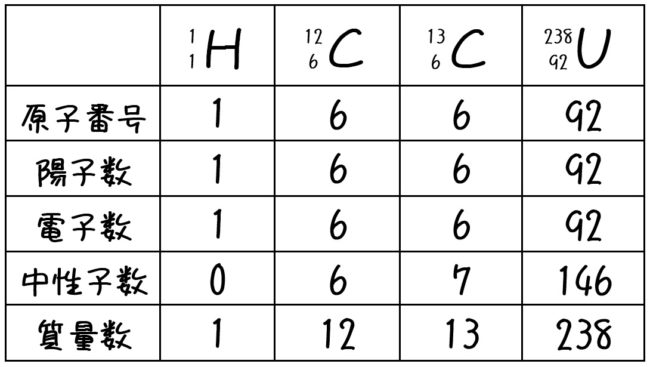



化学基礎 原子の構造 原子番号 質量数 Tekibo



21世紀の自然科学 エネルギーと熱 第4部 原子力エネルギー 正確に理解するための最小限の材料を提供し 私の意見は最後に話します Ppt Download




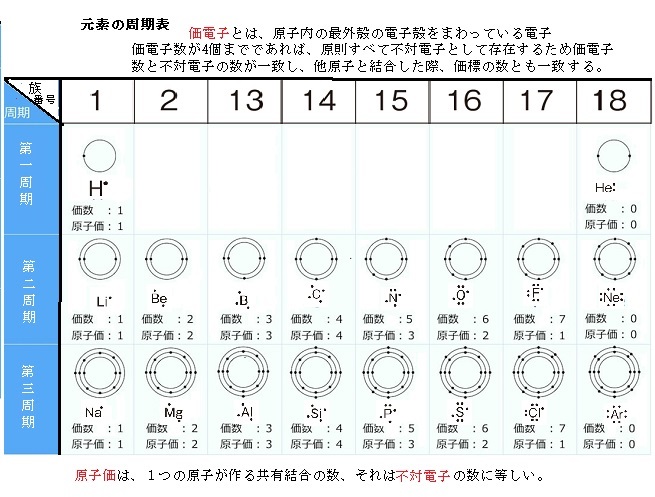
高校化学基礎 周期律と価電子 映像授業のtry It トライイット



車山高原レア メモリーが語る 元素の周期表



Chapter1 1



Numb016
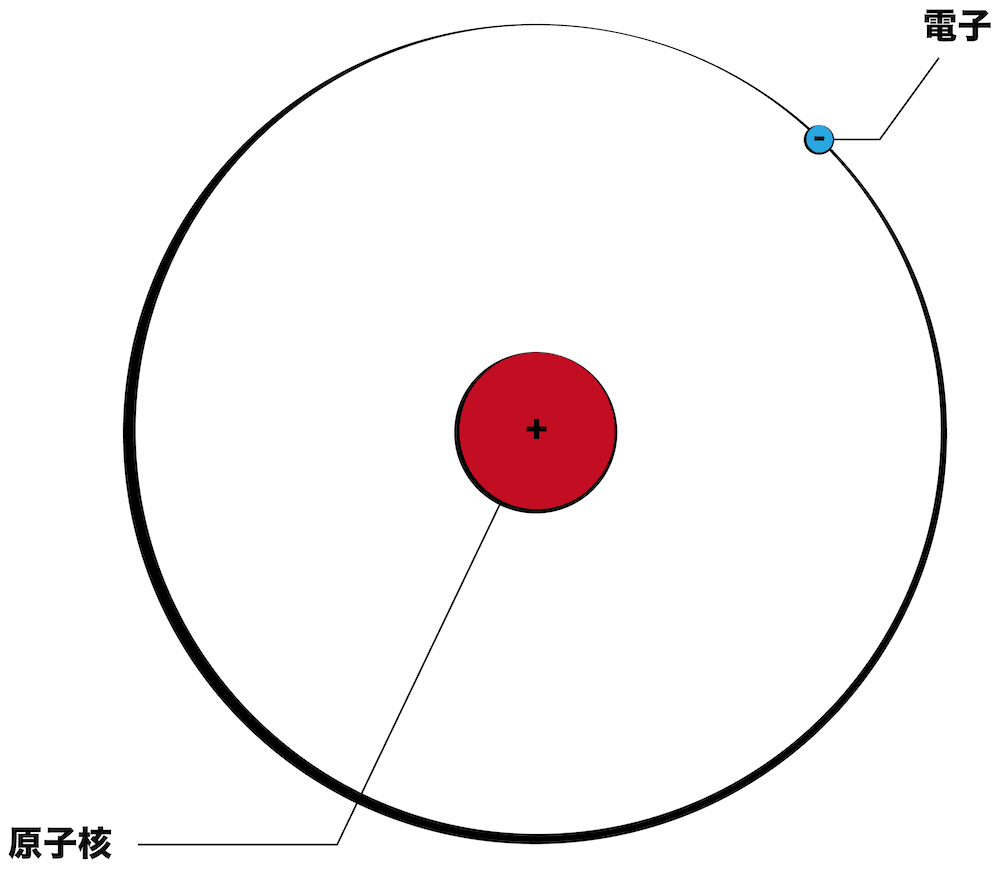



原子の構造 陽子 中性子 電子 原子核 質量数 原子番号の数と関係 化学のグルメ



なんとなくわかる高校化学 M殻とn殻のなぞ
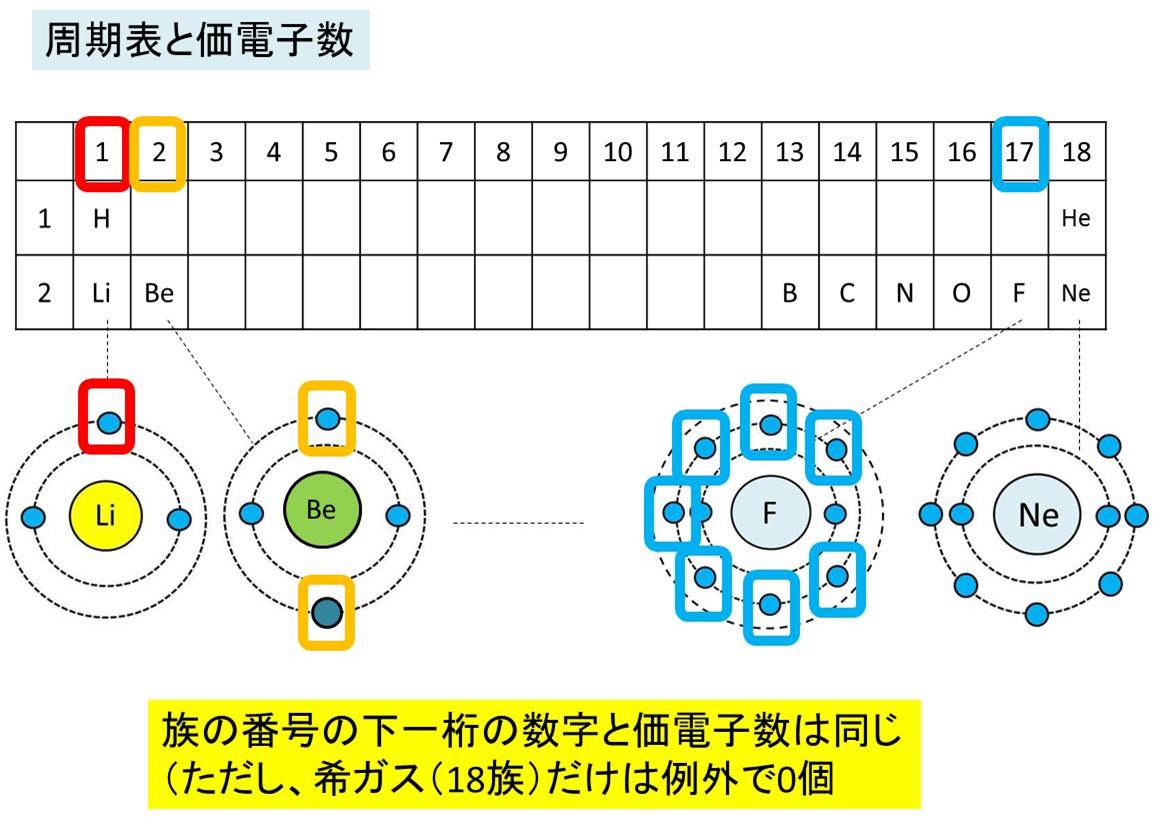



価電子とは 数え方や覚え方 最外殻電子との違いは




目で見て操作する 分子の世界 そのミクロ構造と物性 原子の構造




高校化学基礎 原子番号と質量数 練習編 映像授業のtry It トライイット




原子の構造 原子番号と質量数の関係 Dr あゆみの物理教室




原子の構成と電子配置 原子番号 電子数 陽子数 質量数 化学 クリボの勉強会 4 Youtube



国際周期表年19にちなんで F フッ素 のお話 トピックス ヒカリラボ Photonてらす



原子番号と価電子数 化学基礎 高校化学net参考書




原子とその構造




化学 原子の構成 周期表 これを読めば時短で簡単に全部わかる Youneed




化学 原子の構成 周期表 これを読めば時短で簡単に全部わかる Youneed
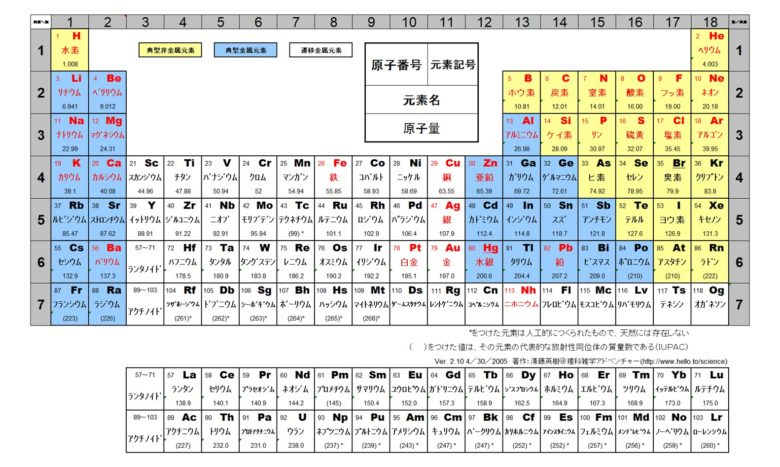



中2化学 原子と分子 中学理科 ポイントまとめと整理




原子核に含まれる陽子の数は 元素ごとに決まっていて 陽子の数と電子の数は等しいと習っ Clear
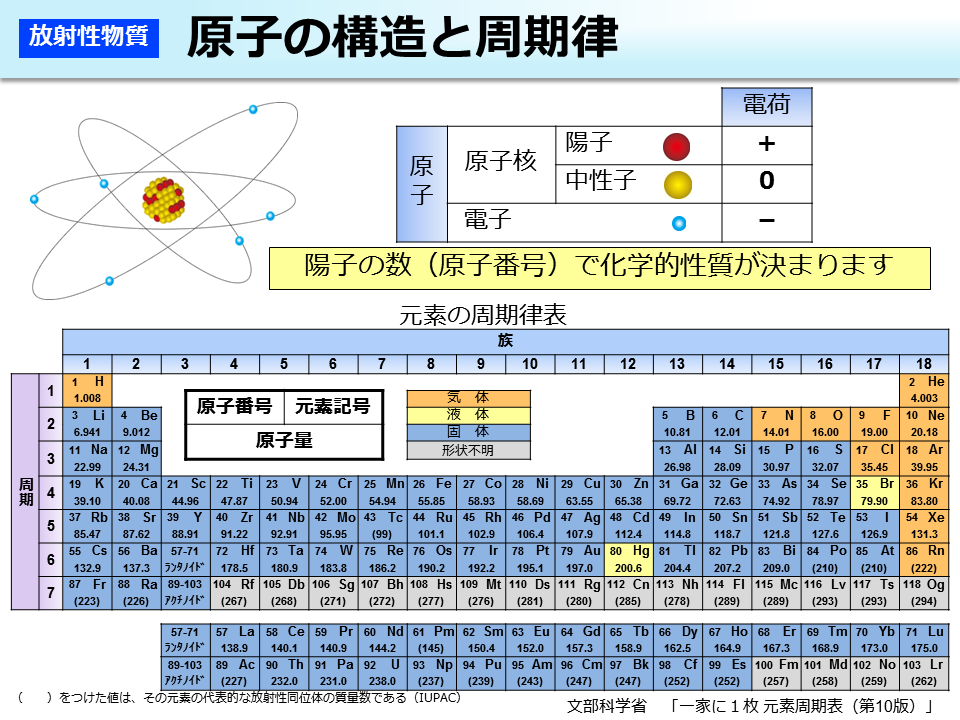



環境省 原子の構造と周期律




高校化学基礎 原子番号と質量数 映像授業のtry It トライイット
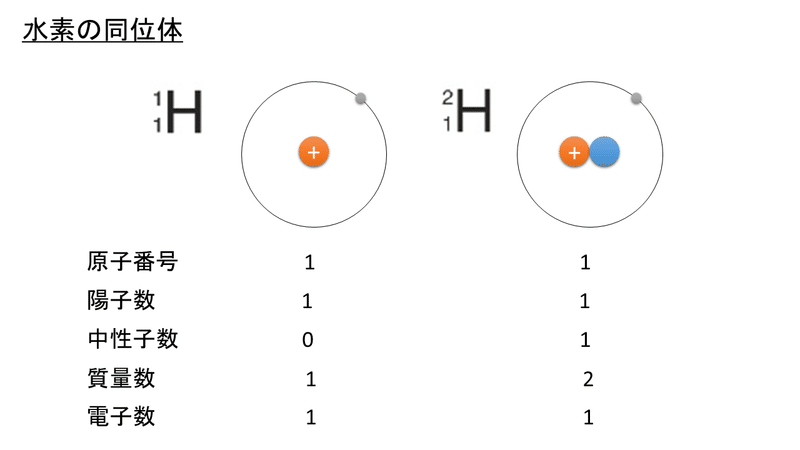



1 3 同位体 おのれー Note
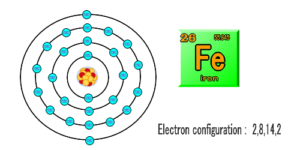



原子と電子の関係 Pochiweb



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Mass Number




原子構造と電子配置 価電子 理系ラボ



Ten Tokyo Shoseki Co Jp Spl Hl Support Files Kou E6 94 B9 E8 A8 E5 8c 96 E5 Ad A6 E5 9f Ba E7 8e 1 E7 A E7 Ab A0 E5 8e 9f E5 Ad 90 81 Ae E6 8b E9 80 A0 81 A8 E5 85 E7 B4 A0 81 Ae E5 91 A8 E6 9c 9f E8 A1 A8 Pdf
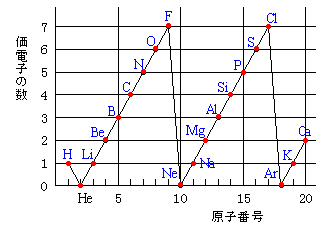



科学 化学 Pararinpoppin In Hell




化学講座 第3回 元素の周期表 私立 国公立大学医学部に入ろう ドットコム




質量数とは 求め方 みんなが知りたい2つの疑問を解消 高校生向け受験応援メディア 受験のミカタ




周期表 Wikipedia




Descubre Como Resolverlo En Qanda



Www Pen Kanagawa Ed Jp Y Meiho H Oshirase Documents 2 Kagakukiso 0508 Pdf
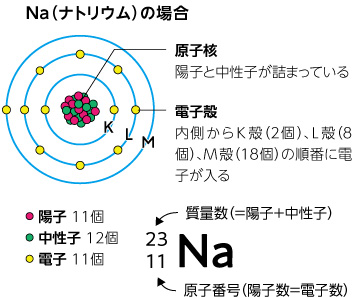



周期表バンザイ Icemsリサーチスコープ 京都大学アイセムス




第1章 原子と原子核の中身について考えよう 放射線について考えよう
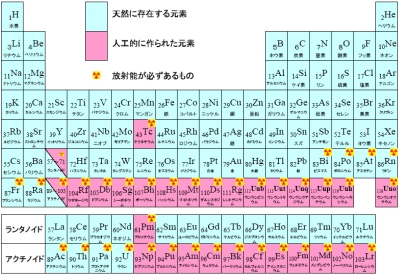



重元素の基礎知識 大阪大学 篠原研究室
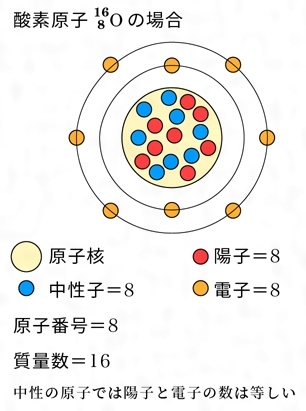



原子とは コトバンク



原子とその構造 化学コラム



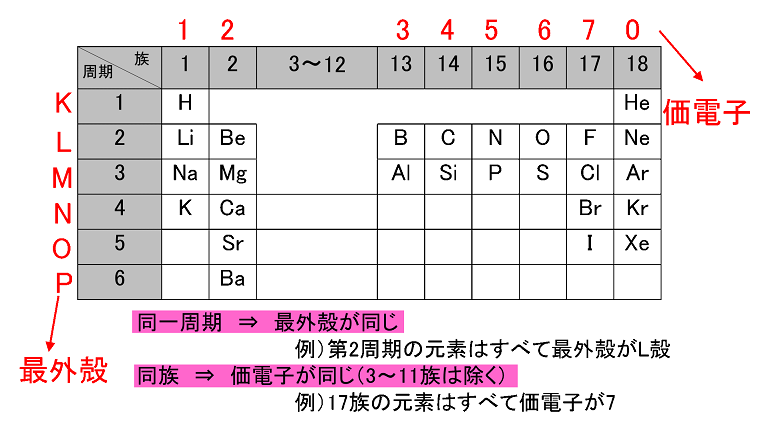
周期表とその見方 戻る 性質のよく似た元素が縦の列に並ぶように整理した表を周期表といいいます 元素の整理 族と周期 同族元素 電子の配置と価電子 価電子とは 最外殻電子の数 4 7 価電子の数 4 7 価電子 最外殻にある1から7個の電子 内側からn




原子核や質量数 同位体の語呂合わせ 陽子数 中性子数 原子番号など 18h30大学入学共通テスト試行調査第2回第1問c 問5 語呂合わせで高校化学 大学入試ゴロ化学




2 79 197 79 56 26 26 30 Descubre Como Resolverlo En Qanda




定期テスト等では 原子番号は提示されないけど 質量数は提示されますよね Clear
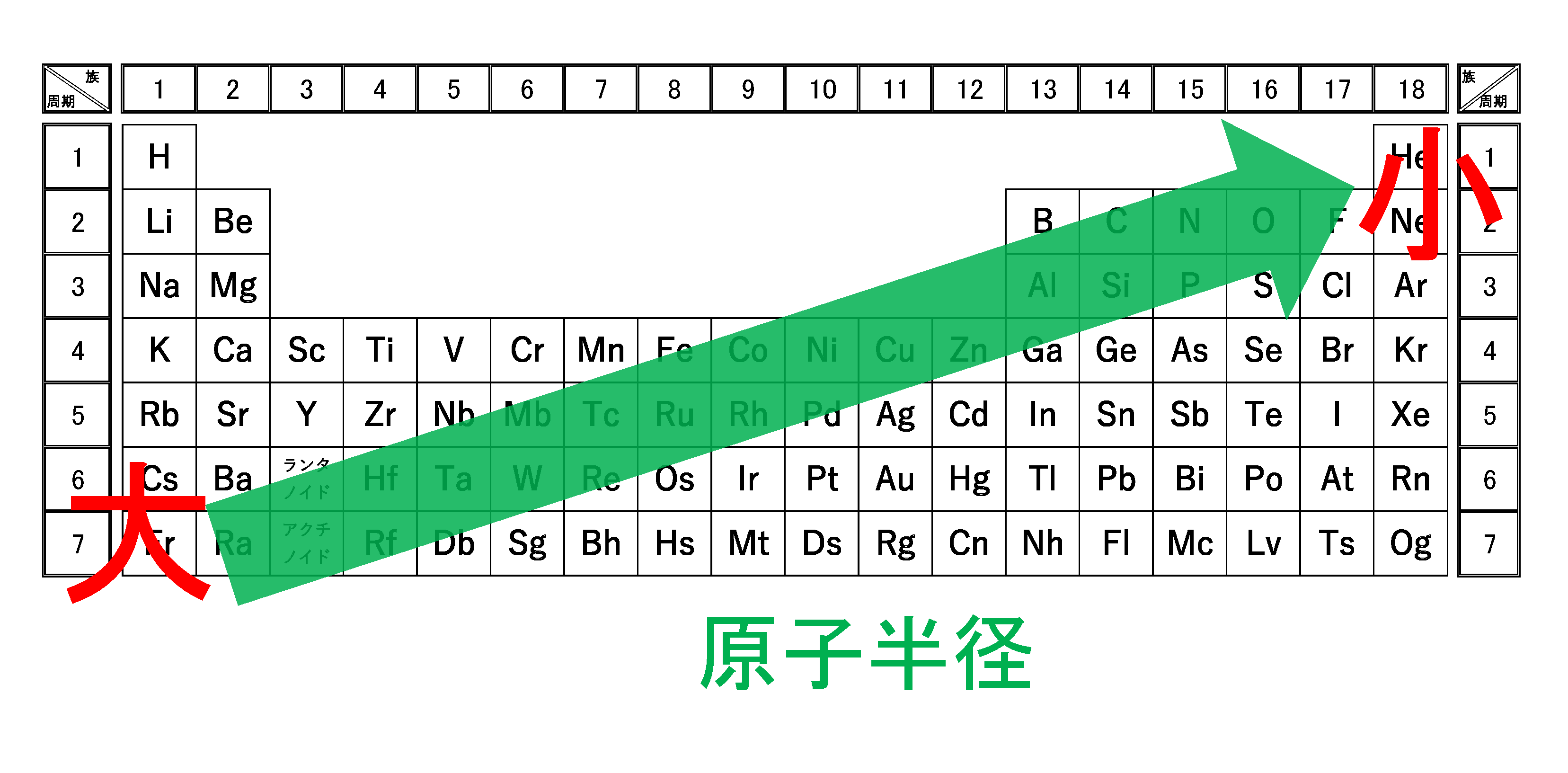



3分でわかる 原子半径 原子の大きさ の周期表での大小関係とその理由を図で徹底解説 サイエンスストック 高校化学をアニメーションで理解する
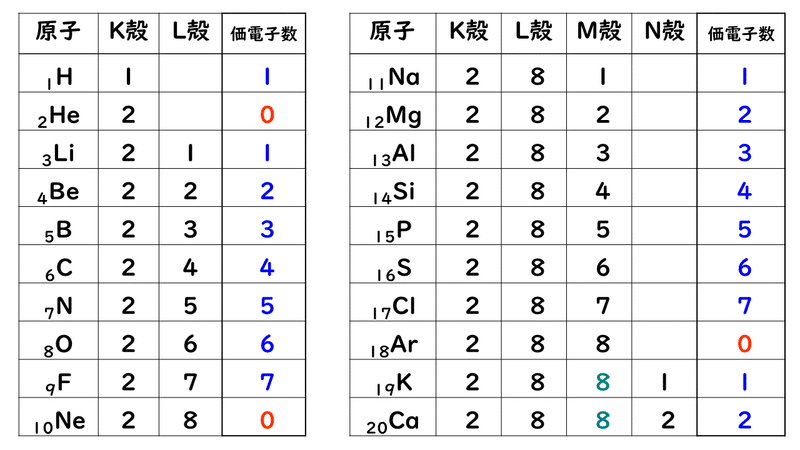



1 4 電子殻と電子配置 おのれー Note




イオンとはそもそも何のこと その1 イオン発見の歴史と原子の構造と原子番号 質量数




3 12 6c 10 13 6c 11 12 1 Descubre Como Resolverlo En Qanda



金とプラチナって何が違うの 結婚指輪の金属をもっと知りたい



化学反応式の書き方




高校化学基礎 周期律と価電子 映像授業のtry It トライイット




大人になって学ぶ 教養としての有機化学 Sur Twitter 原子番号と質量数 原子番号 原子がもつ陽子の数 質量数 原子がもつ陽子と中性子の 数を足したもの 原子番号n番の原子は一般に 陽子をn個 電子をn個 中性子をn個 くらい もっています 例 原子番号6番の炭素 C
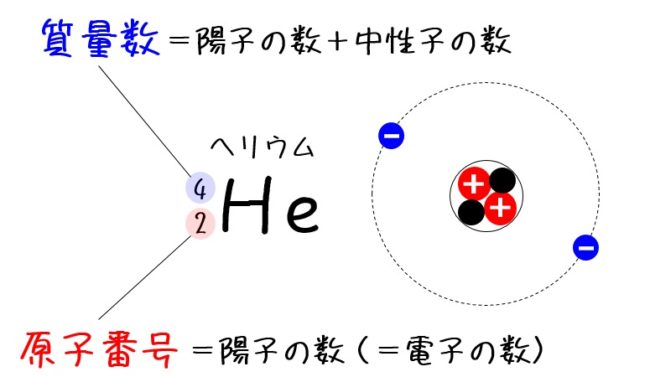



化学基礎 原子の構造 原子番号 質量数 Tekibo



質量数 Mass Number Japaneseclass Jp




図解版 原子 分子 元素の違いと原子の構造を解説 陽子 中性子 質量数 原子番号 サイエンスストック 高校化学をアニメーションで理解する
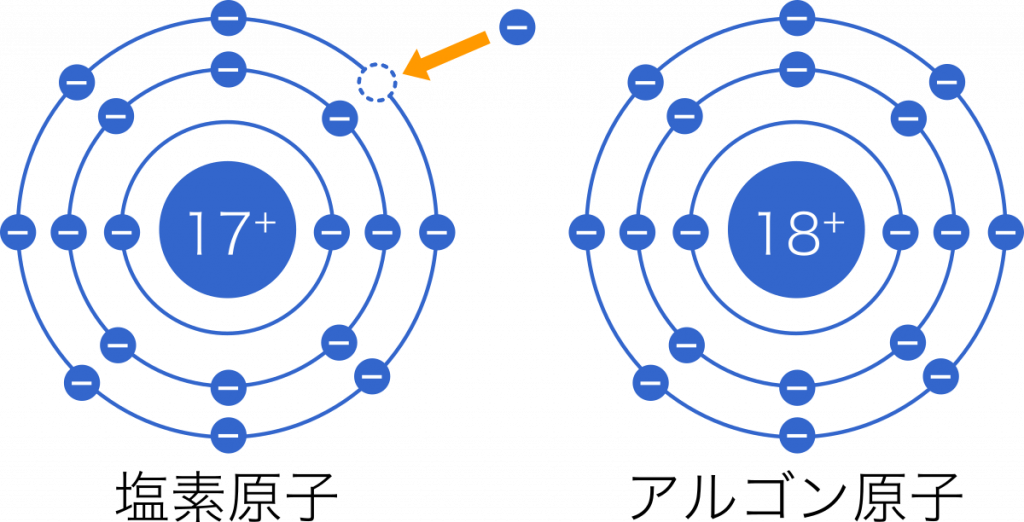



高校化学基礎まとめ イオン Mm参考書
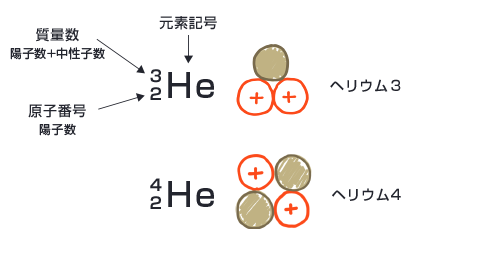



第1章 原子と原子核の中身について考えよう 放射線について考えよう




元素周期表 見やすい表で覚え方と元素を解説 ゴロ合わせも 高校生向け受験応援メディア 受験のミカタ
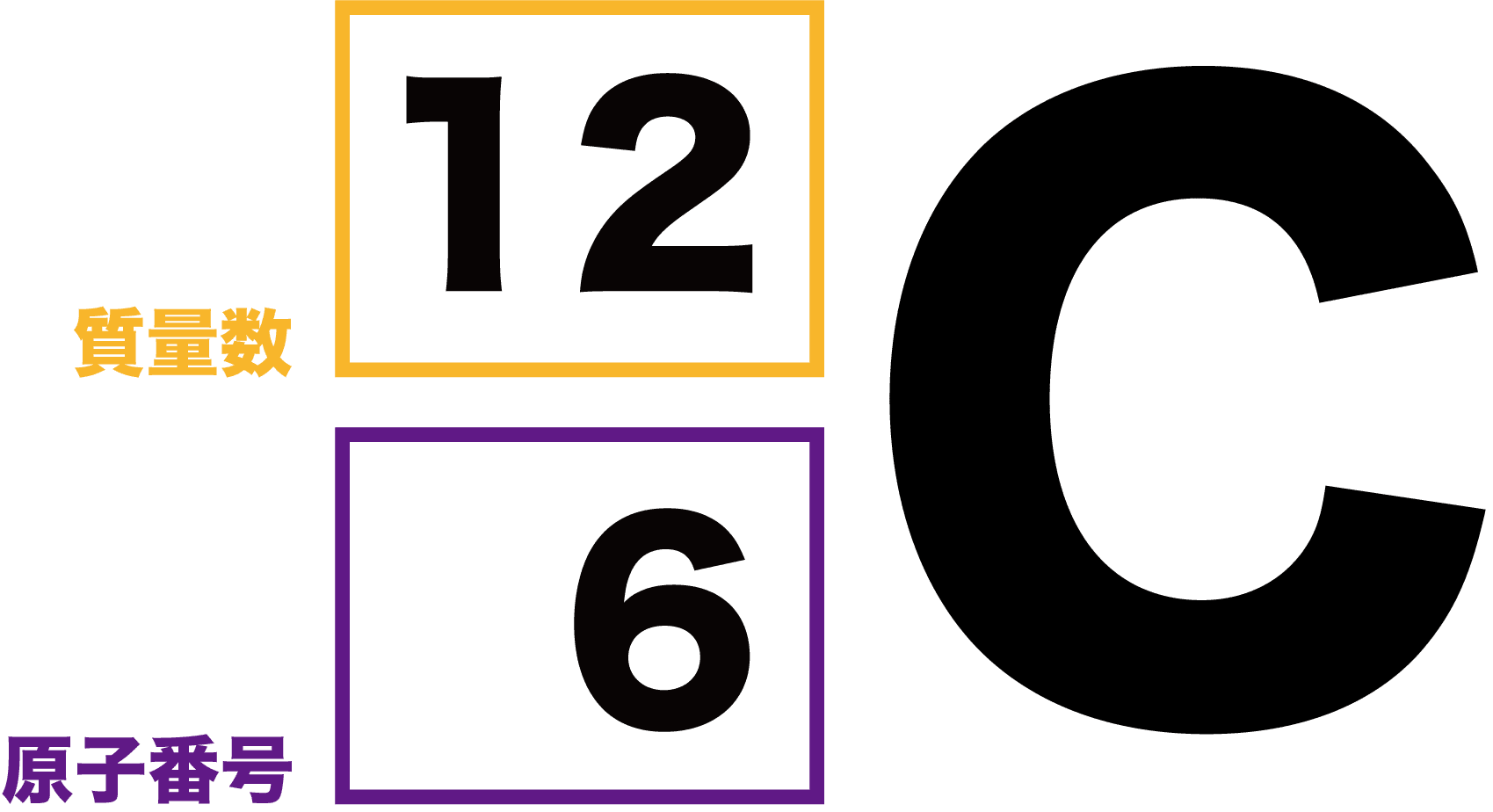



原子の構造 陽子 中性子 電子 原子核 質量数 原子番号の数と関係 化学のグルメ



1 2 原子の構造 おのれー Note



原子の電子配置 電子殻と電子数



全文公開 原子 と 原子核 ってどんなもの 12 24 明日香出版社 公式 Note



図解 電子配置の書き方の解説と電子配置の一覧 周期表 サイエンスストック 高校化学をアニメーションで理解する



周期表を解説 電子配置から周期表を作る 受験メモ



化学基礎 原子の構造 原子番号 質量数 Tekibo



化学 原子 分子の構造と重さ 原子番号



1



宮崎技術研究所 の技術講座 電気と電子のお話 4 1 1



3 12 6c 10 13 6c 11 12 1 Descubre Como Resolverlo En Qanda



原子とその構造



Www Zkai Co Jp Wp Content Uploads Sites 15 19 09 Qcs5a1z1a2 Pdf



Numb016



基礎化学1 物質の構成と物質量




5分でわかる 陽イオン 陰イオン 単原子イオン の価数の考え方と覚え方 電子配置を図で解説 サイエンスストック 高校化学をアニメーションで理解する




原子核に含まれる陽子の数は 元素ごとに決まっていて 陽子の数と電子の数は等しいと習っ Clear



国際周期表年19にちなんで F フッ素 のお話 トピックス ヒカリラボ Photonてらす



1
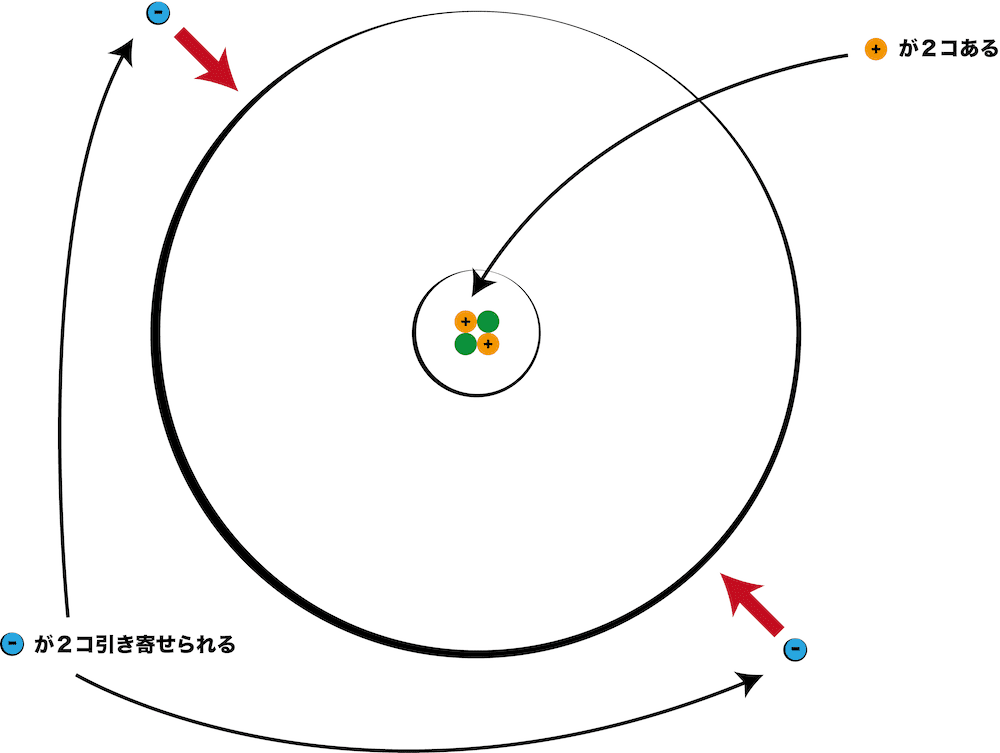



原子の構造 陽子 中性子 電子 原子核 質量数 原子番号の数と関係 化学のグルメ
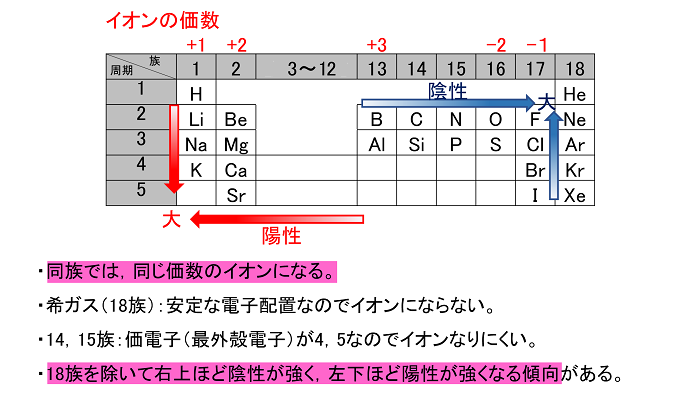



イオン



原子番号 Z 質量数 A 密度r G Cm3 の物質 放射線技師問題集
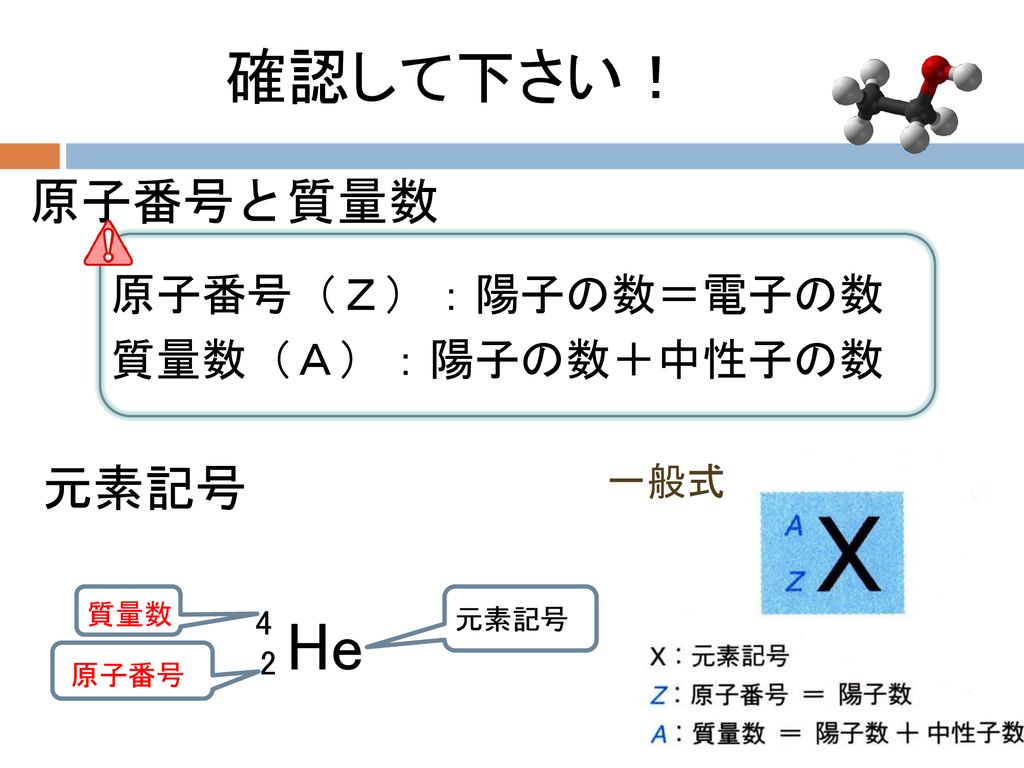



教養の化学 第4週 2013年10月14日 担当 杉本昭子 Ppt Download



1



87ut2q Qnoh4tm
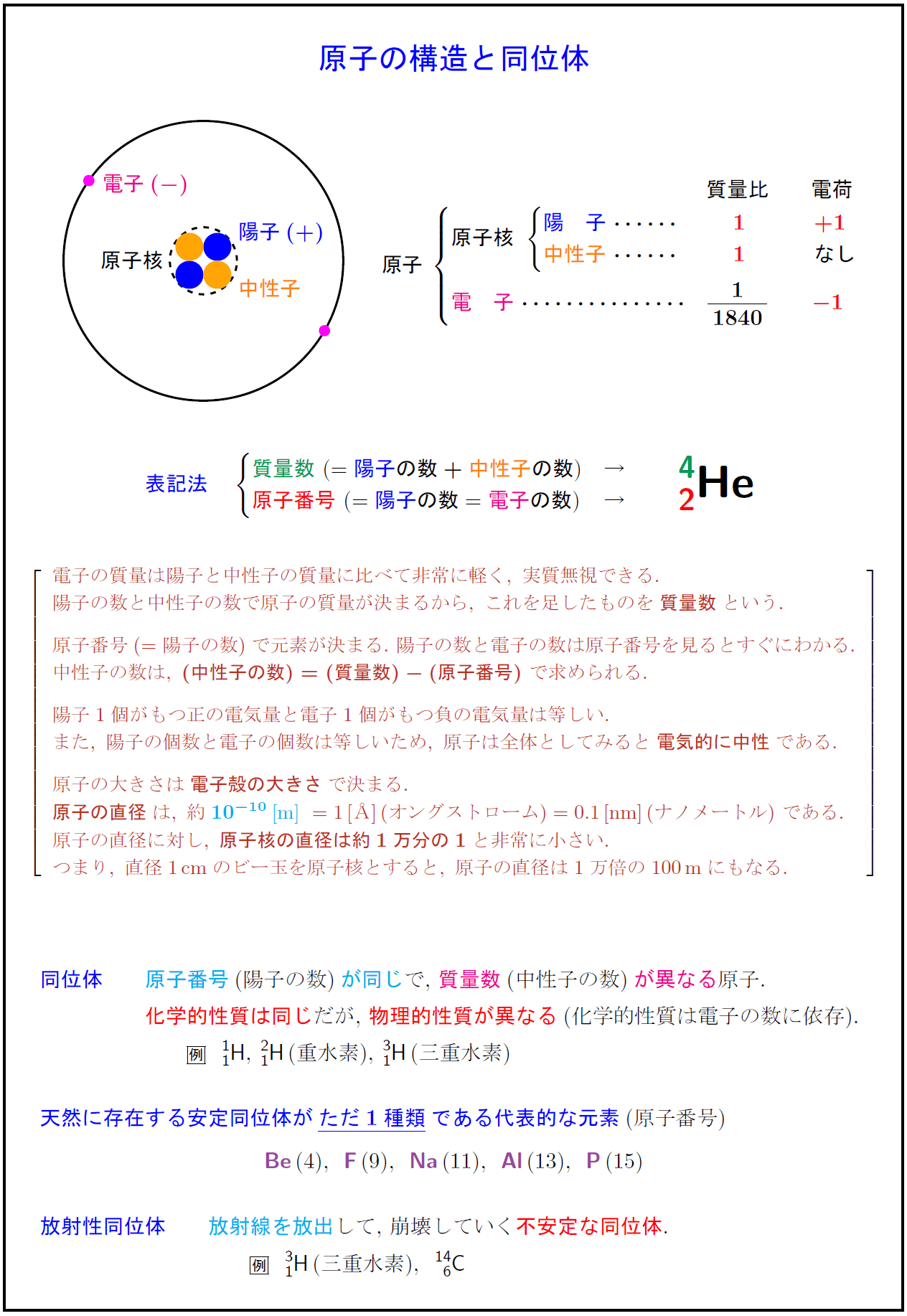



高校理論化学 原子の構造と同位体 受験の月


コメント
コメントを投稿